Dra. María Elina Serra*
Nociones de epidemiología en tiempos de COVID-19
RESUMEN
Las nociones básicas de epidemiología resultan hoy, en la pandemia de COVID-19, necesarias para poder analizar y definir medidas de prevención y contención adecuadas a nivel individual, regional y global.
En este artículo se revisan los pasos para un abordaje sistemático de las situaciones de epidemia, con un detalle de los parámetros epidemiológicos mínimos para ello. Se ofrece también un panorama de las múltiples aristas que presenta una situación de crisis sanitaria, las herramientas con las que se cuenta y los interrogantes que permanecen abiertos.
Palabras clave: epidemiología, COVID-19, salud pública, epidemia.
ABSTRACT
Basic notions of epidemiology are necessary to analyze and define adequate prevention and containment measures at individual, regional and global levels during the COVID-19 pandemic. This article reviews the steps for a systematic approach to epidemic situations with detail of the minimum epidemiological parameters for this. It also offers an overview of the multiple edges presented by a health crisis situation, the tools available and the questions that remain open.
Keywords: epidemiology, COVID-19, public health, epidemic.
Cómo citar:
Serra ME. Nociones de epidemiología en tiempos de COVID-19. Rev Enferm Neonatal. Agosto 2020;33:3-9.
INTRODUCCIÓN
La epidemiología es el estudio de la distribución de las enfermedades en las poblaciones y de los factores que influyen en esa distribución. Su propósito es brindar claves que permitan entender y abordar los cambios en la salud de una población.1,2
Aunque sus antecedentes se remontan a la Edad Antigua, está completamente vigente en el contexto de la pandemia de COVID-19. Clásica, aparentemente estática y poco amigable, hoy todos necesitamos comprender algunas de sus nociones básicas para analizar la situación regional y global y establecer conductas adecuadas para el cuidado de cada paciente, de nosotros mismos y de la comunidad en general.
A continuación se revisan conceptos fundamentales que permiten recorrer el camino del conocimiento sobre el COVID-19, infección nueva para todos, cuya extensión exige respuestas y acciones rápidas y efectivas en pos de minimizar sus consecuencias.
Hay una serie de pasos necesarios para abordar en forma sistemática y efectiva el brote local, regional o global de una enfermedad:
1. Definir la situación.
2. Examinar la distribución de los casos según el lugar y el tiempo.
3. Establecer las variables que implican un mayor riesgo.
4. Desarrollar hipótesis sobre la patogenia.
5. Recomendar, establecer y evaluar medidas de control.3
Se presenta este orden con fines didácticos, pero se trata de un fenómeno dinámico, que requiere revisar una y otra vez cada uno de los puntos mencionados (tabla 1).
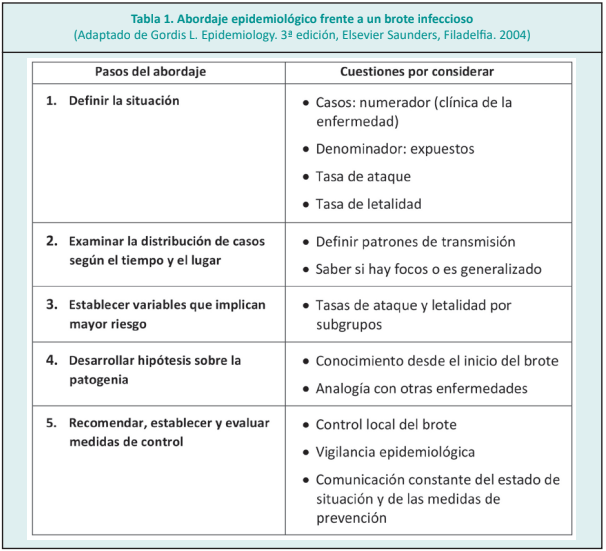
Definir la situación
La primera cuestión por resolver es saber de qué se trata lo que está sucediendo. Para ello es necesario conocer el número de casos. Aunque impresione un tema simple, no lo es si se considera que deberá definirse con precisión las características de los casos sospechosos y el método y puntos de corte para confirmar los mismos. Esto implica al menos una primera aproximación a las particularidades clínicas y microbiológicas de la infección. A partir de esto habrá que preguntarse si se comprenden o conocen las causas, al menos parcialmente.
En esta instancia se tomarán como referencia casos o series de casos, estudios cuya representatividad es por naturaleza limitada, pero de enorme valor como un primer aporte.
Aun conociendo el número de casos nuevos eso no ofrece información suficiente respecto de la magnitud del fenómeno. Imaginemos, por ejemplo, que 100 casos nuevos de una enfermedad pueden ser muchos o pocos solo en relación con el número de potenciales casos nuevos, es decir de aquellos que están expuestos y son susceptibles de enfermar. Entonces corresponde calcular el denominador. Cuando se conoce qué proporción de los expuestos están infectados, hay una idea más certera de la carga de salud pública que implica el problema. Y es con estos datos, con los que es posible definir si se trata de una epidemia.4,5
Con esa información, casos nuevos en un determinado período en relación con la población “expuesta” o en riesgo, puede calcularse la tasa de ataque. La misma es simplemente una tasa de incidencia (casos nuevos entre personas expuestas, durante un período de tiempo) pero en la que la población entera de interés está expuesta y que considera un período más corto que los habitualmente usados (por ejemplo: un día). 6
Los epidemiólogos pueden graficar la evolución de los nuevos casos en el tiempo a través de una curva.7 Cabe aclarar que tratándose de un nuevo agente etiológico, para el que no existe inmunidad en la población, se espera que esa curva vaya aumentando en altura con el correr del tiempo, hasta llegar al momento en el que una determinada proporción de la población ya no sea susceptible de infectarse porque cursó la enfermedad y desarrolló inmunidad o porque falleció. La pendiente de esa curva, es decir la cantidad de casos nuevos en el tiempo (o dicho de otra manera, la velocidad de diseminación) dependerá por un lado de algunas condiciones propias del germen, de condiciones de la población y de las medidas que se adopten frente a esto.
Para contar con un panorama más completo de la situación es de interés también indagar respecto de la gravedad de los casos. El indicador más certero para ello es la tasa de letalidad (“case fatality rate” en inglés). Ésta representa el porcentaje de personas con una determinada enfermedad que fallecen por esa causa en un período de tiempo y en un lugar. Pero debe también notarse aquí que la definición de caso, que en este cálculo está representada en el denominador, condicionará el resultado. En el caso del COVID-19, desde un punto de vista estrictamente teórico, la tasa de letalidad más precisa fue la calculada en el crucero Diamond Princess, pues allí se conocía perfectamente el denominador de expuestos. Sin embargo no puede desdeñarse que esa estimación estará siempre influida por la edad promedio de la muestra y sus comorbilidades, por lo que no resulta generalizable.8
También debe notarse que en el inicio de una situación de brote, sin importar cuán extendido sea el mismo, se incluyen en el denominador solamente los casos “obvios”, por desconocerse el espectro clínico completo de la infección, con lo que esta tasa suele sobreestimarse. Al pasar el tiempo, afectarse más pacientes y comprobarse más ampliamente las manifestaciones de la enfermedad, hay un conocimiento más preciso de quiénes constituyen el denominador; éste se acrecienta y entonces “disminuye” la tasa de letalidad.4
A estas cuestiones hay que sumar dos dificultades adicionales que se presentan en la práctica: la primera corresponde al hecho de que los cálculos podrían estar afectados por las características propias del método de testeo que se aplique (sensibilidad y especificidad del test). La segunda, relacionada con la tasa de letalidad, y más difícil de resolver, es que es necesario discernir entre quienes fallecen a causa de la enfermedad y aquellos que fallecen estando infectados, pero por otra causa.5
Examinar la distribución de los casos según el lugar y el tiempo
La distribución natural de casos en el espacio y el tiempo es útil para determinar:
• La fuente de la infección.
• El nivel de contagiosidad.
• El período de incubación y de contagio.
• Si existen varios focos concretos de infección, o si la
diseminación es generalizada.
Esta información, que surge de la vigilancia epidemiológica necesaria en el contexto de un brote, no solamente aporta datos sobre la dinámica de transmisión de la enfermedad, sino que aproxima a la identificación del germen causante y su origen.
De estos datos depende el poder realizar una estimación inicial respecto de cómo se comportará ese brote. El tiempo de incubación y el nivel de gravedad al inicio del cuadro clínico podrán facilitar o dificultar la contención del brote. Por ejemplo, en el caso del SARS-1, el tiempo de incubación es relativamente corto y la enfermedad se presenta grave desde su inicio,9 entonces hay poco tiempo para que quien esté infectado circule por la comunidad de un modo inadvertido. Para el caso del COVID-19, por el contrario, la incubación es de varios días, muchos infectados cursan en forma oligo- o asintomática y aun quienes desarrollan cuadros graves inician el episodio con síntomas leves de varios días de duración. Así, el tiempo de circulación en la comunidad, de personas que podrían diseminar la infección, es mayor. El conocimiento de estos patrones de transmisión permite orientar las medidas para contenerlo.10
La identificación del germen, que en principio puede aportar la epidemiología, se completa con la determinación de las características del virus que incluyen sus principales proteínas y la secuenciación de su material genético. Estos pasos son necesarios para desarrollar estrategias terapéuticas y de vacunas. En la actualidad pueden hacerse en un tiempo relativamente corto: en el caso del coronavirus 2, los primeros casos se comunicaron en diciembre de 2019 y en enero de 2020 se pudo establecer cuál y cómo era el agente causal. 9
Establecer las variables que implican un mayor riesgo
A partir de las publicaciones de las primeras series de casos y de estudios descriptivos se podrá estimar la asociación entre algunos factores del huésped y las distintas manifestaciones y nivel de gravedad del cuadro clínico. La edad, el sexo y las comorbilidades que clásicamente se relacionan con determinadas enfermedades similares a la de la epidemia en cuestión son las primeras en ser evaluadas.11
También es útil el cálculo de las tasas de ataque y de letalidad para diferentes subgrupos, según surja de la información recabada. Esta estratificación del riesgo permite evaluar la necesidad de establecer medidas de prevención específicas por subgrupos, como es el caso, por ejemplo, de los adultos mayores en relación a la infección por coronavirus 2.
Desarrollar hipótesis sobre la patogenia
A medida que avanza la recolección de datos respecto del comportamiento epidemiológico de la infección, y una vez identificado el agente causal, se desarrollarán diferentes hipótesis respecto del comportamiento de éste en cuanto a su infectividad, manifestación clínica y a los mecanismos patogénicos. Esto surge de la observación y de las analogías entre el nuevo germen y otros similares previamente conocidos. Estas hipótesis deberán examinarse a la luz de nuevos estudios de investigación. Los diseños del tipo casos y controles, que comparan sujetos con y sin enfermedad y permiten valorar la asociación de ese resultado con varios factores de exposición o características previas del sujeto, son útiles para explorar estas especulaciones.
Recomendar, establecer y evaluar medidas de control
La situación de crisis sanitaria que implica un brote infeccioso y que es mayor cuanto más extendido sea, exige la implementación de un programa de contención o mitigación. Cuando no ha sido posible la contención del foco inicial y el impacto del mismo torna no factible el trazado y seguimiento de los contactos cercanos de cada infectado, es necesario establecer medidas de control. Las primeras de ellas son las medidas físicas, que tienen como propósito evitar el contacto entre infectados y no infectados. Dentro de ellas se inscriben las medidas personales de higiene o de limpieza y desinfección de elementos, así como la distancia física, el uso de elementos de protección personal, la cancelación de eventos grupales, el cierre de caminos y fronteras, el trabajo remoto, el cierre de escuelas y el aislamiento social preventivo.9 La vigilancia epidemiológica será la herramienta para valorar la efectividad de estas medidas.
También se consideran medidas necesarias la adecuada comunicación del riesgo, de las formas de transmisión y de las medidas de prevención que coadyuvan para una implementación efectiva de estas últimas.
Otro grupo de medidas son las dirigidas a disminuir la infectividad de los contagiados. Esto incluye las prácticas de control de infecciones dentro de las instituciones sanitarias y el uso eventual de antivirales, que tendrían además el propósito de mejorar los resultados individuales en cuanto al tiempo de hospitalización y a la gravedad de la enfermedad. Aunque podría discutirse la posibilidad del uso compasivo, en situaciones de estado crítico, el uso de estos fármacos está supeditado a la posibilidad de comprobar su eficacia y seguridad, para lo cual es necesario realizar ensayos clínicos, que también requieren de tiempo. Para el caso del COVID-19, el 21 de febrero de 2020 se inició el primer ensayo y actualmente se encuentran en curso más de 1300 estudios de intervención, aún sin resultados concluyentes. 12
El último nivel de medida posible es la reducción de la susceptibilidad, es decir, las vacunas. Si bien sería deseable que fuese lo primero, los tiempos que conlleva la identificación microbiológica, la investigación de su seguridad y eficacia y la producción en cantidad, hace que la vacuna esté entre las últimas medidas factibles de implementar y que su aparición sea, en general, posterior a la resolución de la pandemia. El 18 de marzo se inició el primer ensayo clínico sobre vacunas par COVID-19. Hay más de 100 vacunas candidatas en diferentes fases de investigación; la más adelantada de ellas es Moderna (ingresando actualmente en la fase 3 de su estudio).12
En la tabla 2 se ofrece un resumen de los conceptos principales en relación a cada nivel de medidas.
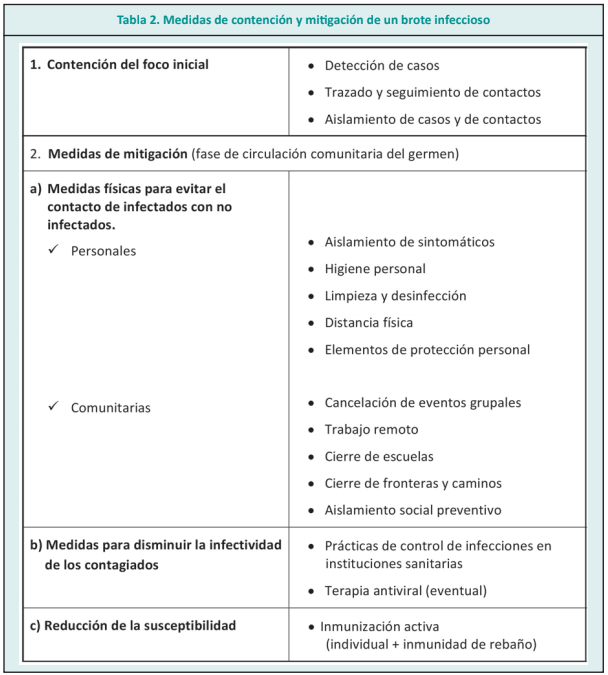
Aprendizajes, incertidumbre e inquietudes
Más de un siglo después de la epidemia de influenza de 1918, vivimos una nueva pandemia, pero contamos con algunas ventajas. Primeramente, conocemos de antemano que los virus con mayor potencial de diseminarse son los que se transmiten eficientemente entre humanos, con períodos asintomáticos suficientemente extensos y con perfiles clínicos inespecíficos. Sabemos cuáles son y que, en su mayoría, son transmitidos desde animales salvajes (con origen en mercados vivos, en general).13 Sabemos que la probabilidad de que sucedan estos brotes ha aumentado y que los factores que favorecen su diseminación incluyen tanto la globalización como las condiciones que debilitan el sistema inmune del huésped y las de la vida en marginalidad (falta de agua potable, falta de cloacas, asentamientos informales).
Los datos sugieren que un enfoque estandarizado para abordar el problema permite investigaciones tempranas para comprender patrones de transmisión, gravedad, características clínicas y factores de riesgo.14 Para ello la OMS brinda formularios modelos que abarcan cuestiones iniciales de estudio como la transmisión entre contactos familiares o los registros clínicos individuales para personas infectadas, entre otras.15 Se enfatiza así la necesidad de definiciones consensuadas que permitan analizar en conjunto la información obtenida por diferentes grupos investigadores en distintas regiones.
Conocemos los tiempos mínimos que conlleva el desarrollo y producción de vacunas eficaces y seguras, pero disponemos de mejor tecnología que en el pasado, incluso de un banco de prototipos de potenciales vacunas sin interés comercial para enfermedades virales, que incluyen el SARS y el MERS, que permitirían abreviar esos procesos.16
Sin embargo, la aplicación de todo aquello que ya conocemos no es sencilla. Hay que esforzarse para adecuar la evidencia al contexto, y establecer políticas de salud aun cuando esa evidencia es incompleta y equívoca.17-19 Prueba de ello es, por ejemplo, el cierre de escuelas. El mismo fue estudiado en la epidemia de gripe H1N1, infección cuyos patrones de transmisión son distintos que los del COVID-19.20 Aunque hasta marzo más de cien países lo implementaron, no hay unanimidad sobre su utilidad o incluso sobre los diferentes modos de llevarlo a la práctica (total, por regiones, solo en grupos donde hay infectados).21
Allí surgen entonces dos inquietudes. La primera es cuánta información epidemiológica es necesaria o es suficiente para implementar una medida. Y la segunda, no menor, son los efectos no deseados de las medidas: el derecho a la salud en equilibrio con el resto de los derechos como trabajar, educarse, etc.22 Así, la puesta en práctica de distintas estrategias es multidisciplinaria, requiere de la epidemiología, pero no se limita a ella.
La disponibilidad de la información científica es también motivo de inquietud y controversia. La urgencia de la situación lleva a que muchas revistas científicas opten por publicar manuscritos antes de su revisión por pares. Aunque se comprende la intención de facilitar la disponibilidad de la evidencia, esto puede dar lugar también a la difusión de resultados no válidos.23
Aun con considerable información en relación al tiempo desde que se inició el problema, nos faltan hoy muchas respuestas. Lo que hace algunos años Oppenheim y colaboradores expresaron en un índice que denotaba si un Estado era capaz de brindar respuesta satisfactoria frente a una epidemia incluía los siguientes factores: infraestructura de salud pública para identificar, trazar y manejar casos y contactos, infraestructura física y de comunicación para canalizar información y recursos, capacidad de gestión pública, posibilidad de movilizar recursos financieros y habilidad para la comunicación efectiva del riesgo.13
Sin embargo, los datos actuales sobre el impacto de la epidemia por COVID-19 en países cuyo índice era satisfactorio sugieren que se necesitan más elementos para sortear de manera efectiva estas situaciones y minimizar el daño.
La pandemia muestra la realidad de nuestra práctica profesional: pocas certezas, muchas preguntas. Es claro que para los profesionales de la salud en este momento las nociones de epidemiología así como los conocimientos que permiten una lectura crítica de las publicaciones científicas, herramientas no siempre valoradas durante la formación, son imprescindibles para la toma de decisiones no solo de salud pública, sino también frente al cuidado y atención del paciente individual y para la efectiva comunicación a la comunidad.
*Doctora en Medicina. Investigadora principal, FUNDASAMIN, Fundación para la Salud Materno Infantil. Programa de Prevención en Salud para Centros de Cuidado Infantil.
Correspondencia: meserra@fundasamin.org.ar
Recibido: 15 de junio de 2020.
Aceptado: 18 de junio de 2020.
Bibliografía
1. Brachman PS. Epidemiology. En: Baron S, editor. Medical Microbiology. 4th edition. Galveston (TX): University of Texas Medical Branch at Galveston; 1996. Chapter 9. [Consulta: 25-06-20]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK7993/
2. Frérot M, Lefebvre A, Aho S, Callier P, et al. What is epidemiology? Changing definitions of epidemiology 1978-2017. PLoS One. 2018 Dec 10;13(12):e0208442.
3. Gordis L. Epidemiology. 3a ed. Philadelphia, Elsevier Saunders, 2004. Chapter 2: The dynamics of disease transmission; p: 15-31.
4. Lipsitch M, Swerdlow DL, Finelli L. Defining the Epidemiology of Covid-19 – Studies Needed. N Engl J Med. 2020;382(13):1194-1196.
5. Pearce N, Vandenbroucke JP, VanderWeele TJ, Greenland S. Accurate Statistics on COVID-19 are Essential for Policy Guidance and Decisions. Am J Public Health. 2020;110(7):949-951.
6. Kelmendi De Ustarán J. Epidemiología. Eudeba, 1o edición. Buenos Aires 1992. Cap. XII: Tasas. Pág: 115-122.
7. Morton RF, Hebel JR, McCarter RJ. A study guide to epidemiology and biostatistics. 5th ed. Maryland, USA: Aspen Publishers; 2001. Chapter I, Investigation of an epidemic; p: 1-5.
8. Rajgor DD, Lee MH, Archuleta S, Bagdasarian N, Quek SC. The many estimates of the COVID-19 case fatality rate [published online ahead of print, 2020 Mar 27]. Lancet Infect Dis. 2020;20(7):776-777.
9. Heymann DL, Shindo N; WHO Scientific and Technical Advisory Group for Infectious Hazards. COVID-19: what is next for public health? Lancet. 2020;395(10224):542-545.
10. Fauci AS, Lane HC, Redfield RR. Covid-19 – Navigating the Uncharted. N Engl J Med. 2020; 382(13):1268-1269.
11. Gordis L. Epidemiology. 3o ed. Philadelphia, Elsevier Saunders, 2004. Chapter 11: Estimating risk: Is there an association? P: 177-190.
12. Del Rio C, Malani P. Translating Science on COVID-19 to Improve Clinical Care and Support the Public Health Response [published online ahead of print, 2020 May 22]. JAMA. 2020;10.1001/jama.2020.9252.
13. Madhav N, Oppenheim B, Gallivan M, Mulembakani P, et al. Pandemic: Risks, Impact and Mitigation. En: Jamison DT, Gelband H, Horton S, Jha P, et al. Disease Control Priorities: Improving Health and Reducing Poverty. 3rd Ed. International Bank for Reconstruction and Development / The World Bank. 2018. Vol. 9. Chapter 17; p: 315-346.
14. Simpson CR, Beever D, Challen K, De Angelis D, et al. The UK’s pandemic influenza research portfolio: a model for future research on emerging infections. Lancet Infect Dis. 2019 Aug;19(8):e295-e300.
15. OMS. Foco técnico: Investigaciones epidemiológicas y clínicas precoces sobre el COVID-19 para una respuesta de salud pública. [Consulta: 25-06-20]. Disponible en: https://www.who.int/emergencies/diseases/novel‐coronavirus-2019/technical‐guidance/early‐investigations
16. Coalition for Epidemic Preparedness Innovation (CEPI). New vaccines for a safer world. [Consulta: 25-06-20]. Disponible en: https://cepi.net/.
17. Gordis L. Epidemiology. 3o ed. Philadelphia, Elsevier Saunders, 2004. Chapter 19: Epidemiology and public policy; p: 301-313.
18. Wensing M, Sales A, Armstrong R, Wilson P. Implementation science in times of Covid-19. Implement Sci. 2020; 15(1):42. Published 2020 Jun 8.
19. Scally G, Jacobson B, Abbasi K. The UK’s public health response to covid-19. Too little, too late, too flawed. BMJ. 2020 May 15;369:m1932.
20. Jackson C, Mangtani P, Hawker J, Olowokure B, Vynnycky E. The Effects of School Closures on Influenza Outbreaks and Pandemics: Systematic Review of Simulation Studies. PLoS One. 2014;9(5):e97297. Published 2014 May 15.
21. Viner RM, Russell SJ, Croker H, Packer J, et al. School closure and management practices during coronavirus outbreaks including COVID-19: a rapid systematic review, Lancet Child Adolesc Health. 2020;4(5):397–404.
22. Lewnard JA, Lo NC. Scientific and ethical basis for social-distancing interventions against COVID-19. Lancet Infect Dis. 2020 Jun;20(6):631-633.
23. Aguilar A. COVID-19. Reflexiones acerca de la abrumadora e indiscriminada información científica y su difusión. Arch Argent Pediatr. 2020;118(4):226-227.













