Dra. Daniela M. Berdullas*, Dra. Gladys Saa**, ELic. Fabiana Sebastiani***
RESUMEN
El dolor neonatal tiene impacto a corto plazo, y altera el neurodesarrollo a largo plazo, por lo cual es importante implementar medidas de confort durante la internación. Hay situaciones en las que las medidas no farmacológicas no son suficientes y es necesario administrar drogas para evitar el dolor en la terapia intensiva neonatal.
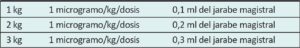
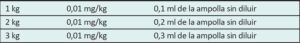
Las diferentes dosis que deben utilizarse según la edad gestacional y el peso del paciente pueden llevar a errores en la administración.
Este artículo aborda un protocolo de sedoanalgesia con estándares de dilución y dosis según la edad gestacional y el peso, con el objetivo de disminuir estos errores.
Palabras clave: dolor, neonato, errores, medidas farmacológicas.
ABSTRACT
Neonatal pain has a short-term impact and alters long-term neurodevelopment; it is important to implement comfort measures during hospitalization. There are situations in which non-pharmacological measures are not enough and it is necessary to administer drugs to prevent pain in the neonatal intensive care unit.
The different doses to be used according to the gestational age and weight of the patient can lead to errors in administration.
This article proposes a sedoanalgesia protocol with dilution and dose standards according to gestational age and weight, with the aim of reducing these errors.
Key words: pain, neonate, errors, pharmacological measures.
Cómo citar:
Berdullas DM, Saa G, Sebastiani. Implementación de estándares de medicación sedoanalgésica en una unidad de cuidados intensivos neonatales. Rev Enferm Neonatal. Abril 2022;38:21-36.
INTRODUCCIÓN:
Con las mejoras y avances en la tecnología aplicada a la recuperación de la salud de los recién nacidos (RN), se ha logrado que cada vez más los neonatos sobrevivan con menor edad gestacional y menor peso. Esto lleva a que neonatos que antes no eran compatibles con la vida, hoy sean pacientes en los diferentes servicios de cuidados intensivos neonatales.
Una vez que nacen, estos niños deben someterse a numerosos procedimientos, como son intubaciones endotraqueales, colocación de catéteres, extracciones de sangre, cirugías y curaciones, que tienen un patrón en común: todos generan dolor.1
Las vías anatómicas y biológicas de transmisión del dolor están presentes y son funcionales en el feto y el RN, mientras que los sistemas fisiológicos de protección ante el dolor son aún inmaduros. Este desequilibrio hace que el neonato presente un umbral bajo de percepción y una capacidad de nocicepción intensa y difusa en el espacio. En el feto se empiezan a formar los receptores nociceptivos a partir de la séptima semana de gestación en la zona peribucal y para la semana 20 estos cubren la totalidad de la superficie corporal del mismo. Estos receptores son terminaciones nerviosas libres localizadas en la piel, los músculos y las vísceras, que se activan por estímulos mecánicos, térmicos y/o químicos, de esta forma recogen los estímulos dolorosos y los transmiten a través de fibras nerviosas sensitivas hasta el asta dorsal de la médula espinal, ascienden y alcanzan el tálamo y, finalmente, la corteza cerebral.
El feto presenta 2 tipos de fibras sensitivas, mielínicas y no mielínicas, y si bien el proceso de mielinización comienza a partir de la semana 22 de gestación, la transmisión del dolor por las fibras amielínicas no se encuentra limitada y para la semana 20-24 se completan las arborizaciones dendríticas y conexiones sinápticas entre la médula, el tronco, el tálamo y la corteza, con lo cual podemos inferir que todos los componentes anatómicos, neurofisiológicos y hormonales necesarios para la percepción del dolor se encuentran completamente desarrollados para el momento que nacen nuestros pacientes.
En el RN y en particular en los recién nacidos pretérmino (RNPT) al ser expuestos a un procedimiento doloroso se desencadena un fenómeno de apoptosis y otras modificaciones a nivel del sistema nervioso central (SNC) además de disminuir el umbral del dolor con lo cual presentan una respuesta mayor y más prolongada al mismo que conduce cambios a largo plazo con gran impacto en el neurodesarrollo.2
Todo lo antes mencionado afecta la evolución de los neonatos internados y aumenta su morbi-mortalidad; si bien con los avances que existen hoy en día y el conocimiento sobre esto, se han implementado diferentes estrategias para lograr disminuir el dolor en los RN, estas son aún ineficaces y dada la difícil evaluación de estos niños y la heterogeneidad de los pacientes en los distintos centros de salud, los mismos terminan siendo insuficientementes tratados. Es por esto que cada unidad de cuidados intensivos neonatales debería implementar un protocolo de prevención y manejo del dolor que incluya estrategias para minimizar el número de procedimientos dolorosos, reducir la exposición a estímulos ambientales (luz y ruidos), aplicar métodos de evaluación de dolor en aquellos pacientes en los que el mismo no pueda ser evitado y estrategias de uso de medidas no farmacológicas y farmacológicas de manera efectiva en aquellos pacientes que lo requieran según los puntajes de evaluación implementados.3
La evaluación de dolor en el RN suele ser un momento desafiante para el personal de salud, ya que se trata de una estimación subjetiva en un sujeto incapaz de poder expresar verbalmente su dolor. Es por esto que se han creado escalas de dolor/sedación, que para ser aplicadas en los diferentes centros debieron ser validadas. Estas evalúan por un lado cambios conductuales y por el otro, cambios fisiológicos (principalmente signos vitales). Cabe destacar que, en los prematuros, la expresión del dolor está más relacionada con estos cambios fisiológicos que con los conductuales, por lo cual algunas escalas validadas para prematuros dan más importancia a la respuesta fisiológica.2
Las escalas más utilizadas son el Sistema de Codificación Facial Neonatal (NFCS: Neonatal Facial Coding System), que evalúa la presencia de dolor en los procedimientos a través de 10 movimientos faciales del bebé: si presenta dicho parámetro se le da 1 punto y si no, 0 puntos. El puntaje máximo son 10 puntos para el RNPT y 9 puntos para el recién nacido de término (RNT). Se hace diagnóstico de que el neonato tiene dolor con un valor > 3 puntos.
El Perfil de Dolor del Prematuro (PIPP: Premature Infant Pain Profile), es de elección en RNT y RNPT (de 28 a 40 semanas) en postoperatorio o ante la realización de algún procedimiento, en la cual se evalúan 7 parámetros; cada uno se evalúa de 0 a 3 y puede alcanzar un valor máximo de 18-21 según el ajuste por edad gestacional. Un valor ≤ 6 indica que el paciente no presenta dolor, y los valores ≥ 12 indican dolor moderado-intenso.
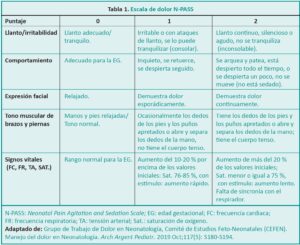
La Escala de Evaluación del Dolor y la Sedación Neonatal (N-PASS: Neonatal Pain Agitation and Sedation Scale), evalúa por separado el dolor y la sedación en los RNT y los RNPT. Evaluación del dolor: el puntaje se registra de 0 a 2 por cada comportamiento y criterio fisiológico. Se adicionan puntos en los RNPT según la EG. El puntaje total se registra como un número positivo (0 a 11), y se debe iniciar tratamiento con los pacientes con puntaje mayor a 3. Evaluación de la sedación: no necesita ser registrada cada vez que se evalúa el dolor. Se asigna 0 a -2 por cada criterio con puntaje total negativo de 0 a -10. Los niveles deseables varían en cada situación: Sedación profunda: puntaje entre -10 y -5. Sedación leve: puntaje entre -5 y -2. Sin sedación: puntaje 0. Un puntaje negativo sin la administración de opiáceos podría indicar que el paciente está expuesto en forma prolongada al dolor, estrés, depresión neurológica, infección u otra patología.
Otras escalas validadas son la de Dolor Agudo del Recién Nacido (DAN: Douleur Aiguë du Nouveau-né) y la de Indicadores de Comportamiento de Dolor Infantil (BIIP: Behavioral Indicators of Infant Pain); ambas evalúan patrones conductuales.2
Si bien en la actualidad con las escalas mencionadas la evaluación del dolor es más objetiva y unificada que antes, sigue estando sujeta a la evaluación del estado del paciente por parte de médicos/as y enfermeros/as por lo que se sigue investigando la posibilidad de métodos más objetivos y específicos aun como la espectroscopía cercana al infrarrojo (near-infrared spectroscopy; NIRS, por sus siglas en inglés), la electroencefalografía de amplitud integrada, la conductancia cutánea y la evaluación de la variabilidad de la FC.2
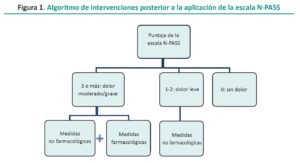
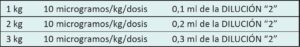
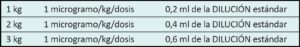
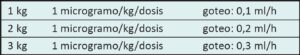
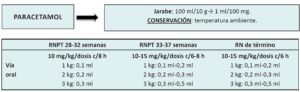
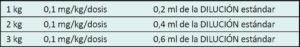
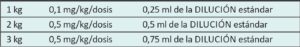
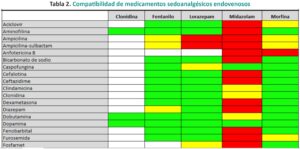
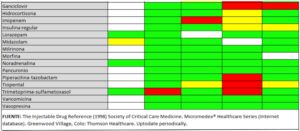
Una vez que se aplica la escala elegida por cada servicio surge la posibilidad de que el neonato se encuentre con dolor moderado/grave con requerimiento de aplicar medidas farmacológicas, las cuales muchas veces llevan a errores en la administración, debido a las diferentes dosis y concentraciones de los fármacos a utilizar, según las distintas edades gestacionales y pesos de los pacientes. Con la estrategia de minimizar estos errores se implementará el siguiente protocolo de administración de medicación sedoanalgésica en una unidad de cuidados intensivos neonatales.