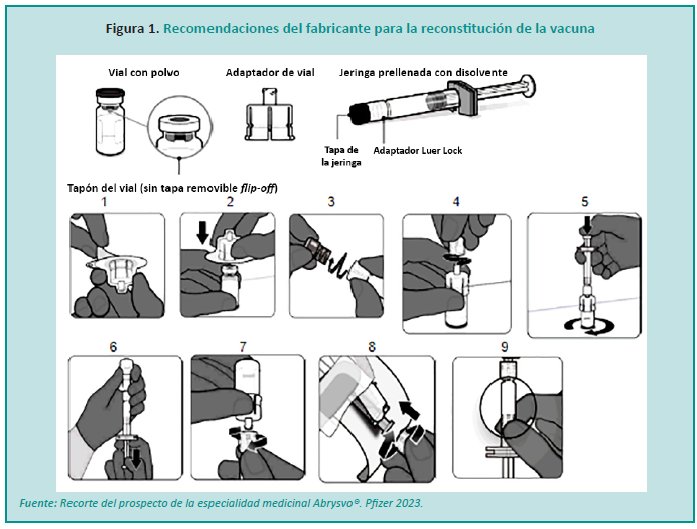
Farm. Abril Maistruarena *
RESUMEN
El virus sincicial respiratorio es uno de los causantes más habituales de bronquiolitis. En Argentina, durante 2023 se registraron 213 165 casos de bronquiolitis, con una incidencia acumulada de 14 611,1 casos/100 000 habitantes. En el mes de septiembre de 2023, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) autorizó la inscripción de una vacuna bivalente contra el virus sincicial respiratorio recombinante, que desde enero de 2024 forma parte del Calendario Nacional de Vacunación.
La misma se contempla para su utilización en mujeres embarazadas entre las semanas 32 y 36 de gestación para la prevención de la enfermedad respiratoria baja y de la forma grave de enfermedad en niños, desde el nacimiento hasta los 6 meses de edad.
El siguiente artículo busca describir los puntos más relevantes de la información sanitaria de esta vacuna, ya que cuando se encuentre disponible lo estará en todos los vacunatorios del país.
Palabras clave: infecciones por virus sincitial respiratorio; vacunas contra virus sincitial respiratorio; embarazo; prevención de enfermedades.
ABSTRACT
Respiratory syncytial virus is one of the most common causes of bronchiolitis. In Argentina, during 2023, 213,165 cases of bronchiolitis were registered, with a cumulative incidence of 14,611.1 cases/100,000 habitants. In September 2023, the National Administration of Medicines, Food and Medical Technology (ANMAT) authorized the registration of a bivalent vaccine against recombinant respiratory syncytial virus; since January 2024 it has been part of the National Vaccination Calendar. It is contemplated for use in pregnant women between 32 and 36 weeks of gestation for the prevention of lower respiratory disease and the severe form of the disease in children from birth to 6 months of age. The following article seeks to describe the most relevant points of health information about this vaccine, since it will be available in all vaccination centers.
Keywords: respiratory syncytial virus infections; respiratory syncytial virus vaccines; pregnancy; disease prevention.
RESUMO
O vírus sincicial respiratório é uma das causas mais comuns de bronquiolite. Na Argentina, durante 2023, foram registrados 213.165 casos de bronquiolite, com uma incidencia acumulada de 14.611,1 casos/100.000 habitantes. Em setembro de 2023, a Administração Nacional de Medicamentos, Alimentos e Tecnologia Médica (ANMAT) autorizou o registro de uma vacina bivalente contra o vírus sincicial respiratório recombio nante, que desde janeiro de 2024 faz parte do Calendário Nacional de Vacinação. Esta vacina é considerada para uso em gestantes entre 32 e 36 semanas de gestação para a prevenção de doenças respiratórias inferiores e da forma grave da doença em crianças, desde o nascimento até os 6 meses de idade. O seguinte artigo busca descrever os pontos mais relevantes das informações de saúde desta vacina, pois quando estiver disponível estará disponível em todos os centros de vacinação do país.
Palavras-chave: infecções por vírus respiratório sincicial; vacinas contra virus sincicial respiratorio; gravidez; prevenção de doenças.
doi: https://doi.org/10.61481/Rev.enferm.neonatal.n44.02
Cómo citar: Maistruarena A. La novedad en material del virus sincicial respiratorio. Rev Enferm Neonatal. Abril 2024;44:14-19.