Prof. Lic. Estela R. Domínguez*
Cardiopatías congénitas en el recién nacido
RESUMEN
Las cardiopatías congénitas son malformaciones que se producen en la anatomía del corazón durante el desarrollo fetal.
Se estima que en Argentina nacen cada año 7000 niños con alguna cardiopatía congénita. Los recién nacidos que no fueron diagnosticados en la etapa prenatal, al momento del nacimiento o durante la evaluación por el profesional de salud, pueden padecer una des-compensación que suele ser brusca, con graves consecuencias y, en ocasiones, con riesgo para la vida.
Los avances tecnológicos permiten obtener un diagnóstico precoz a partir de las 20 semanas de gestación y, a su vez, que todo el equipo de salud pueda adelantarse y programar el tratamiento y/o la intervención quirúrgica en centros con la infraestructura adecuada a la cardiopatía.
Este artículo aborda generalidades del cuidado de los neonatos con cardiopatía congénita de acuerdo a su clasificación.
Palabras clave: cardiopatías congénitas, cianóticas, acianóticas, cortocircuito, cuidados de enfermería.
ABSTRACT
Congenital heart diseases are malformations that occur in the anatomy of the heart during fetal development.
It is estimated that 7,000 children with some congen-ital heart disease are born each year in Argentina. Newborns who were not prenatally diagnosed, may suffer a decompensation that is usually abrupt, with serious consequences and, sometimes life-threatening, at birth or during the medical evaluation.
Technological advances allow an early diagnosis after 20 weeks of gestation and, in turn, the entire health team can get ahead and schedule treatment and/or surgery in centers with adequate infrastructure for heart disease.
This article deals with generalities of neonatal care of infants with congenital heart disease according to their classification.
Keywords: congenital heart disease, cyanotic, acya-notic, shunt, nursing care.
Cómo citar:
Domínguez E. Cardiopatías congénitas en el recién nacido, Rev Enferm Neonatal. Abril 2019;30:4-16.
Desarrollo
Las cardiopatías congénitas (CC) son malformaciones que se producen en la anatomía del corazón durante el desarrollo fetal. Es la malformación congénita más frecuente y la segunda causa de muerte en el periodo neonatal, responsable de más del 10 % de la mortalidad infantil.1,2 Uno de cada cien recién nacidos (RN) presenta alguna cardiopatía congénita; en Argentina nacen al año unos 7000 niños con esta patología3
Los avances tecnológicos, especialmente las bioimágenes, permiten obtener un diagnóstico precoz. Desde las 20 semanas de gestación es posible detectar una cardiopatía congénita.1 La detección temprana brinda a todo el equipo multidisciplinario las herramientas necesarias para adelantarse a posibles problemas, permite nuevas intervenciones terapéuticas y técnicas quirúrgicas para la reparación de las cardiopatías más complejas. Los profesionales de enfermería, especializados y capacitados, cumplen un rol fundamental en la planificación de los cuidados pre y posoperatorios. Además, individualizan al sujeto de atención, hacen posible una supervivencia prolongada, no solo al evitar complicaciones quirúrgicas sino también mejorando la morbimortalidad asociada.
Clasificación de las cardiopatías congénitas
Existen numerosos tipos de CC y diversas formas de clasificarlas. Las manifestaciones clínicas y el momento de presentación son diferentes según el tipo de defecto. El RN durante las primeras semanas o meses de vida puede estar asintomático o por el contrario pre-sentar graves síntomas incompatibles con la vida.4
Un tipo de clasificación de las CC, que suele utilizarse para su mejor comprensión y según el modo de presentación en el RN, es el que tiene como criterio la presencia o ausencia de cianosis, coloración azulada de la piel que suele indicar un bajo nivel de oxígeno en la sangre;5 se discriminan así, anomalías cianóticas y acianóticas. A su vez, estas últimas se subdividen según su fisiopatología (Tabla 1).
Dentro de las CC cianóticas se encuentran las que suponen una disminución del flujo pulmonar u obstrucción del corazón derecho, las que son consecuencia de la mezcla total o completa entre el retorno venoso sistémico y el pulmonar, y la falta de mezcla de la transposición entre los circuitos sistémico y pulmonar. Este grupo de CC es el más heterogéneo siendo su característica común el shunt de derecha a izquierda.6
Entre las CC acianóticas se encuentran las cardiopatías con shunt de izquierda a derecha, las cardiopatías obstructivas de corazón izquierdo y otras menos frecuentes como son las insuficiencias valvulares o las miocardiopatías.6
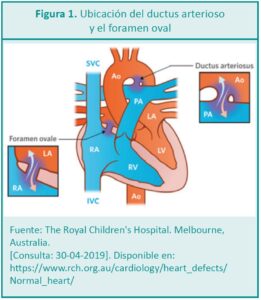
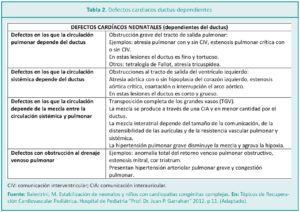
En el período neonatal suelen manifestarse la mayoría de las cardiopatías congénitas complejas derivadas de los cambios de la circulación. En el periodo fetal, la circulación pulmonar y sistémica presenta una disposición paralela, donde ambos ventrículos perfunden simultáneamente a ambos territorios mediante el foramen oval y el ductus arterioso (Figura 1). La disposición hemodinámica y los desvíos del flujo sanguíneo (shunt) permiten que las cardiopatías graves pasen desapercibidas hasta el nacimiento. Cuando el ductus y el foramen tienden a cerrarse (Figura 2), se separa la circulación derecha de la izquierda y se establece la circulación en serie.2 El intercambio de gases, que era realizado exclusivamente por la placenta, es asumido por los pulmones del RN que no eran funcionales hasta ese momento.7

Cortocircuito y shunt
El desvío de sangre por una comunicación anormal del corazón, manteniendo el flujo, desde una red de alta resistencia a una red de menor resistencia, se denomina shunt en idioma inglés.
En los textos científicos en idioma castellano se utiliza el término “cortocircuito” para ese desvío de la sangre aunque no son sinónimos, dado que “cortocircuito” implica la interrupción de un flujo (el flujo eléctrico). Sería más adecuado utilizar el término “desvío”.8 Dado que refleja mejor la dinámica de esta situación, en adelante utilizaremos el término shunt.
Shunt de izquierda a derecha
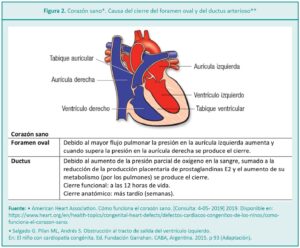
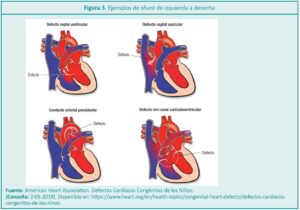
El shunt de izquierda a derecha (I-D) hace referencia al paso de sangre oxigenada desde el lado izquierdo del corazón (aurícula izquierda, ventrículo izquierdo, o aorta) hacia el lado derecho de éste (aurícula derecha, ventrículo derecho, o arteria pulmonar), sangre que recircula por los pulmones sin entrar a la circulación arterial sistémica periférica.9 En las cardiopatías en donde se presenta este tipo de shunt (Figura 3) es importante tener en cuenta que puede cambiar la dirección debido a cambios en la resistencia vascular pulmonar u obstrucciones fijas o dinámicas distales al sitio donde se encuentra el shunt.6
Durante las primeras semanas de vida la resistencia pulmonar se encuentra elevada, impidiendo que en este período el shunt sea masivo.
Hay ciertos factores que influyen en la magnitud del shunt, entre ellos, los siguientes:
• Hemoglobina: a menor concentración de hemoglobina mayor shunt; esto se debe a la viscosidad de la sangre y su efecto en la resistencia vascular.
• Sobrecarga de volumen y dilatación de las cavidades cardiacas.9
Cuadro clínico
Entre los hallazgos más característicos se encuentra la acumulación de líquido intersticial pulmonar que produce taquipnea; se origina en el hiperflujo pulmonar inicial y, en la mayoría, puede aumentar a dificultad respiratoria. Esto genera propensión a cuadros infecciosos respiratorios recurrentes.6,9
La disminución del flujo sistémico genera la respuesta compensatoria neurohumoral que produce taquicardia, sudoración y aumento del gasto energético, entre otros.
Otra consecuencia es la sobrecarga de volumen y la dilatación de las cavidades cardiacas. La magnitud del shunt se refleja en el grado de aumento del tamaño cardíaco.
La contractibilidad del miocardio está generalmente conservada o incluso aumentada considerando el incremento de la precarga por la sobrecarga de volumen. También se encuentra un precordio hiperactivo y un soplo cardíaco caracterizado como holosistólico en la comunicación interventricular (CIV) o sistólico en la coartación de aorta.
La hepatomegalia es consecuencia del aumento de presiones diastólicas de las cavidades derechas y la congestión venosa sistémica producidas por el aumento de la presión arterial pulmonar.
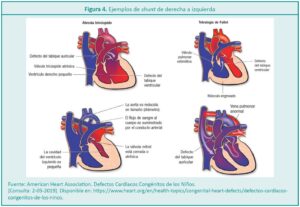
Shunt de derecha a izquierda
La característica común en el shunt de derecha a izquierda (D-I) es la hipoxemia que se manifiesta clínicamente a través de la cianosis de piel y mucosas6 y su consecuencia es el insuficiente aporte de oxígeno a los tejidos para satisfacer los requerimientos metabólicos. Cualquier situación que disminuya bruscamente la resistencia vascular sistémica o que incremente la resistencia pulmonar provoca aumento del shunt de derecha a izquierda como ocurre durante el llanto o la defecación.9
En las cardiopatías en donde se presenta este tipo de shunt (Figura 4) hay un aumento de presión en el lado derecho del corazón junto con la presencia de una comunicación ya sea auricular, ventricular o aortopulmonar a través de las cuales la sangre desaturada del lado derecho pasa al circuito sistémico, excepto en la transposición de los grandes vasos.10,11
La cianosis marcada de piel y mucosas desde las primeras horas de vida o posterior al cierre del ductus arterioso, es el resultado de la desaturación de más de 3 g/dl de hemoglobina de la sangre arterial, no asocia-da a dificultad respiratoria, sino solo con hiperpnea.6,9
La cianosis puede ser central o periférica. Es central, cuando la desaturación ocurre por shunt a nivel cardíaco o pulmonar y es periférica si ocurre por un aumento de la extracción de oxígeno tisular en relación a flujos lentos en la circulación periférica como en el gasto cardíaco (GC) disminuido, la presión venosa elevada o la policitemia.
En el examen cardiovascular se observan pulsos normales, precordio quieto, segundo ruido y soplo característico de acuerdo a la CC. En la tetralogía de Fallot se ausculta un soplo sistólico, en la atresia pulmonar con CIV el soplo es continuo. El tamaño cardíaco es normal como en la tetralogía de Fallot o la estenosis pulmonar, o aumentado como en el canal aurículoventricular, la atresia tricuspídea o la atresia pulmonar con septum íntegro.
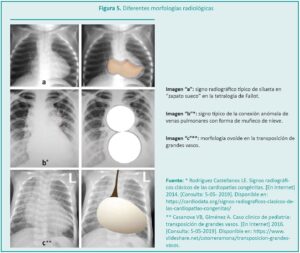
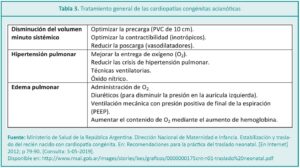
La silueta del corazón varía de acuerdo a la CC. Ejemplo de ello es la forma de bota o zueco en la tetralogía de Fallot, el formato ovoide en la transposición de las grandes arterias o con aspecto de muñeco de nieve en la conexión anómala de venas pulmonares (Figura 5). La vasculatura pulmonar puede estar normal o disminuida.
Tratamiento
Las CC que requieren cateterismo o cirugía de urgencia, como la anomalía total del retorno venoso pulmonar (ATRVP) obstructiva o la hipoplasia de ventrículo izquierdo con septum interauricular intacto, requieren el nacimiento en centros de alta complejidad o su inminente derivación a ellos.12
Las CC que dependen del mantenimiento del ductus permeable deben iniciar el tratamiento en la UCIN con un goteo de prostaglandinas.12
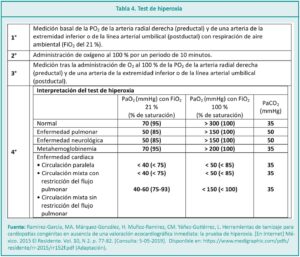
Las estrategias terapéuticas en las CC acianóticas dependerán de la clínica y de la fisiopatología de presentación. Se deberá considerar principalmente la disminución del volumen minuto sistémico, la hipertensión pulmonar y el edema pulmonar (Tabla 3).
Las estrategias diagnósticas y terapéuticas en las CC cianóticas comienzan con el diagnóstico diferencial, o sea determinar si el origen de la cianosis es otro, como una enfermedad pulmonar, el síndrome de hiperten-sión pulmonar persistente del RN o la metahemoglo-binopatía (cianosis con saturación y PaO2 normal que requiere tratamiento específico).12
El test de hiperoxia (Tabla 4) ayuda a determinar el origen de la cianosis; la hipoxemia se define como la PO2 arterial menor de 60-70 mmHg respirando oxígeno al 100 % por un período de 10 minutos.11.12 La oximetría de pulso no debe ser nunca utilizada para la interpretación del test de hiperoxia debido a que no puede detectar el incremento de la PO2 arterial (curva de disociación de la Hb).13 Cuando existe un gran shunt derecha-izquierda el aumento de la PO2 con administración de oxígeno es escasa o nula.11.14
La administración de oxígeno en el RN con cianosis debe realizarse con monitorización permanente y se debe evaluar la respuesta en cada caso sobre todo conociendo que el exceso de oxígeno puede ser nocivo por la producción de superóxidos y radicales libres. También se debe recordar que el exceso de oxígeno puede ocasionar el cierre del ductus o el descenso brusco de la resistencia pulmonar.15
Una diferencia ≥ 5 % entre el oxímetro de pulso colocado en la mano derecha (preductal) y los miembros inferiores también certifica hipertensión pulmonar.12
La radiografía de tórax se utiliza para delimitar el tamaño del corazón y determinar si la vasculatura pulmonar se encuentra incrementada o disminuida. Con el electrocardiograma (ECG) se evalúa la frecuencia cardíaca, el ritmo, el eje, los intervalos, la progresión de las ondas R, ondas P y la morfología de las ondas ST/T, a la vez que ayuda a determinar si hay isquemia, dilatación auricular o hipertrofia ventricular.13
El ecocardiograma es un método de diagnóstico no invasivo muy eficaz para evaluar la anatomía cardiovascular y la función miocárdica, el tipo de defecto y su repercusión hemodinámica.
Detección de cardiopatías congénitas por oximetría de pulso
La oximetría de pulso es utilizada para detectar a RN con algún grado de hipoxia, cuya causa podría ser una cardiopatía congénita o bien alguna alteración no cardíaca que pudiera poner en riesgo al recién nacido. Es una intervención sencilla, no invasiva, realizada por parte del personal de enfermería en pocos minutos en todos los recién nacidos después de las 24 horas de vida. La detección dentro de las primeras 24 horas de vida no es tan específica como la detección posterior porque la hipoxemia ocurre comúnmente durante la transición de condiciones de vida intrauterina a extrauterina. La oximetría de pulso no consigue detectar todos los casos de CC críticas o de CC cianóticas pues la hipoxemia puede no estar presente en algunos RN antes del alta hospitalaria. 11,18-20
Una detección oportuna sin diagnóstico prenatal, permite una pronta estabilización, tratamiento y/o derivación antes de que aparezcan los signos y síntomas.17 Es adecuada para decir que un RN no tiene la patología buscada (prueba negativa) por la altísima especificidad (99,9 %) pero menos confiable cuando resulta positivo (sensibilidad del 76 %).18
Tratamiento
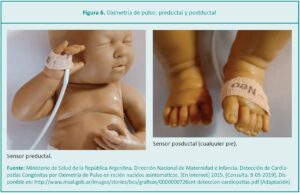
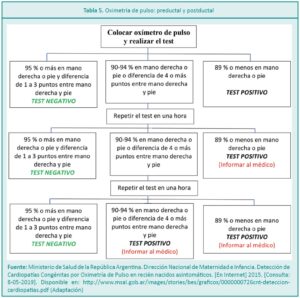
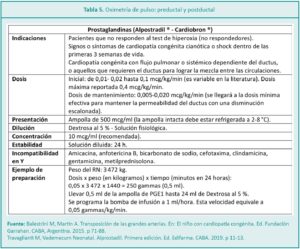
• El personal de enfermería coloca el oxímetro de pulso utilizando solo un sensor neonatal en la mano derecha (preductal) del paciente y luego se lo colocará en cualquiera de los dos pies (postductal) hasta obtener una lectura confiable (Figura 6). Es necesario obtener estos dos registros para la realización del test (Tabla 5).
RESULTADOS
• Test negativo: los valores de saturometría son mayores o iguales al 95 % y la diferencia entre la mano derecha y el pie es de 3 puntos o menos.
• Test positivo: la saturación en la mano derecha o cualquiera de los dos pies es menor o igual al 89 %. Se debe comunicar el resultado al médico tratante para iniciar la evaluación e identificación de la causa de la hipoxemia.
• Cuando los valores de saturometría sean entre el 90-94 % o con una diferencia entre la mano derecha y el pie mayor o igual a 4 puntos, se deberá repetir la prueba después de 1 hora siguiendo los criterios iniciales. Si no se define en la segunda lectura se recomienda realizar una tercera lectura 1 hora después de la segunda. Si, luego de la tercera lectura, la prueba sigue dando entre el 90 % y el 94 %, o con 4 puntos o más de diferencia entre la mano derecha y el pie, la prueba será considerada positiva y se debe proceder en consecuencia.17
Control de la vía aérea
Es necesario mantener una buena ventilación y administrar oxígeno suplementario para mantener la saturación entre el 75 % y el 85 %. Ante la presencia de dificultad respiratoria, alteración del sensorio, apneas y/o shock, se debe evaluar la intubación y la asistencia ventilatoria mecánica.
También se debe tener en cuenta la gravedad de la cianosis, la inestabilidad hemodinámica, la edad gestacional (EG) y la distancia a recorrer en caso de requerir derivación a otro centro. La sedación en el paciente ventilado permite reducir el consumo de oxígeno, aumentar la saturación venosa y mejorar la entrega de oxígeno.12,14
Control de la vía aérea
La primera opción en el RN es la canalización de los vasos umbilicales. El catéter umbilical venoso se utiliza para la administración de soluciones y fármacos y el catéter umbilical arterial para controlar la tensión arterial invasiva y la extracción de sangre necesaria para valorar el medio interno y la oxigenación, sin realizar repetidas punciones.14
La utilización de percutáneas de uno o dos lúmenes es una opción en la UCIN cuando no es posible la canalización umbilical o no se encuentra en la ubicación correcta. Una o dos vías periféricas, según la cantidad de lúmenes centrales disponibles, serán necesarias para administrar el plan de hidratación (PHP), sedación, analgesia o expansiones.
Administración de medicamentos
La prostaglandina E1 (PGE1) es clave en el tratamiento del RN con CC ductus-dependientes; aun sin certeza de diagnóstico, puede salvar la vida del niño hasta alcanzar la consulta especializada o la derivación. Su acción previene o revierte el cierre funcional del ductus al mejorar el flujo pulmonar en las lesiones obstructivas derechas, el flujo sistémico en las lesiones obstructivas izquierdas y la mezcla a través del ductus permeable en las lesiones con circulación en paralelo. Se administra por vía endovenosa central preferente-mente, diluida, en forma continua, mediante bomba de infusión. En la (Tabla 6) se pueden visualizar recomendaciones para la administración de este medica-mento.11,12,15,16
La respuesta es inmediata cuando el ductus es importante para la hemodinamia del RN. Cuando no hay respuesta (en los llamados “no respondedores”), en neonatos más grandes es debido a la ausencia de ductus o a la obstrucción el retorno venoso. El deterioro con la administración de PGE1 es infrecuente y resulta muy útil para el diagnóstico de CC con obstrucción en la desembocadura de las venas pulmonares o salida de la AI como la anomalía del retorno venoso pulmonar de tipo obstructivo o la transposición de grandes arterias con foramen oval restrictivo. Estas represen-tan una emergencia y requieren cateterismo o cirugía de urgencia.12,15
Los efectos adversos de la PGE1 son: fiebre (14 %), apneas (10-12 %), rubefacción (10 %), hipotensión (3-4 %), convulsiones (4 %), taquicardia (3 %), diarrea (2 %), sepsis (2 %) y, por debajo del 1 %, arritmias, sibilancias y anuria, entre otros. Son más intensos en el RN pretérmino y más frecuentes en RN menores de 2000 g. Habitualmente aparecen en las primeras horas de la infusión. Ante un RN con infusión de este medicamento se deben realizar controles frecuentes de presión arterial, frecuencia respiratoria, frecuencia cardíaca, temperatura, pH y PO2. También se debe contar con los recursos disponibles para iniciar una eventual asistencia respiratoria.11,12,14-16
Agradecimiento
A la Dra. Analia Martín por la revisión.
Los padres del recién nacido con cardiopatía congénita
Las intervenciones de enfermería deben propiciar una relación de confianza desde el principio, promover la participación en los cuidados diarios, utilizar un lenguaje adaptado al contexto de la familia y siempre explicar los procedimientos antes de realizarlos. Es importante proveer información y aclarar dudas sobre el diagnóstico, el tratamiento y las normas del servicio, en lo posible a través de instructivos escritos, considerando que las diferentes emociones concurrentes durante la internación pueden disminuir la retención de la información y la comprensión.
Iniciar la formación de los padres en el rol de cuidador, durante la hospitalización es un desafío, sobre todo cuando se instala la idea de una enfermedad prolongada que puede generar secuelas y requerir cuidados especiales en el hogar por un periodo indeterminado.
CONCLUSIÓN
El profesional de enfermería es un integrante del equipo multidisciplinario y su quehacer diario es de suma importancia para la recuperación del neonato con CC a través de cuidados eficientes y oportunos. También debe coordinar acciones con el resto del equipo de salud y favorecer la participación activa de la familia durante la internación.
* Prof. Lic. en Enfermería. Enfermera asistencial del Servicio de Cirugía Cardiovascular (CCV-UCI 35), Hospital de Pediatría “Prof. Dr. Juan P. Garrahan”.
Correspondencia: dominguezestela.r@gmail.com
Recibido: 4 de mayo de 2019
Aceptado: 4 de junio de 2019
Bibliografía
1. McNichol L, Lund C, Rosen T, Gray M. Medical adhesives and patient safety: state of the science: consensus statements for the assessment, prevention, and treatment of adhesive-related skin injuries. Orthop Nurs. 2013; 32(5):267-281.
2. McManus Kuller J. Skin breakdown: Risk factors, prevention and treatment. Newborn and Infant Reviews. 2001; 1:35-42.
3. McNichol L, Lund C, Rosen T, Gray M. Medical adhesives and patient safety: state of the science: consensus statements for the assessment, preventyion, and treatment of adhesive-related skin injuries. Orthop Nurs. 2013; 32(5):267-81.
4. Konya C, Sanada H, Sugama J, Okuwa M, et al. Skin injuries caused by medical adhesive tape in older people and associated factors. J Clin Nurs. 2010; 19(9-19):1236-42.
5. Habiballah L. Prevalence of neonate adhesive skin injuries in a Jordanian intensive care unit. Nurs Child Young People. 2017; 29(10):42-46.
6. Lund C, Kuller J, Lane A, Lott JW, Raines DA. Neonatal skin care: the scientific basis for practice. J Obstet Gynecol Neonatal Nurs. 1999; 28(3):241-54.
7. Darmstad GL, Dinulus JG. Neonatal skin care. Pediatr Clin North Am. 2000; 47(4):757-82.
8. Afsar FS. Skin care for preterm and term neonates. Clin Exp Dermatol. 2009; 34(8):855-8.
9. US Food & Drug Administration (FDA). Medical adhesive tape and adhesive bandage. [Consulta: 01-02-21]. Disponible en: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?FR=880.5240
10. McNichol L, Lund C, Rosen T, Gray M. Medical adhesives and patient safety: state of the science: consensus statements for the assessment, prevention, and treatment of adhesive-related skin injuries. J Wound Ostomy Continence Nurs. 2013; 40(4): 365-80.
11. Bryant RA. Types of skin damage and differential diagnosis. In: Bryant R, Nix D, editors. Acute & chronic wounds: current management concepts. 5th ed. St Louis, MO: Elsevier; 2016.p.82-108.
12. Lund CH, Nonato LB, Kuller JM, Franck LS, et al. Disruption of barrier function in neonatal skin associated with adhesive removal. J Pediatr. 1997; 131(3):367-72.
13. Taroc AM. Staying out of sticky situations: how to choose the right tape for your patient. Am Nurse Today. [Internet]. 2015;10(7). [Consulta: 06-03-21]. Disponible en: https://www.myamericannurse.com/staying-sticky-situations/
14. Zulkowski K. Understanding Moisture-Associated Skin Damage, Medical Adhesive-Related Skin Injuries, and Skin Tears. Adv Skin Wound Care. 2017; 30(8):372-381.
15. Institute for Healthcare Improvement (IHI). Bundles. [Consulta: 01-02-21]. Disponible en: tp://www.ihi. org/sites/search/pages/results.aspx?k=bundles.
16. Lund CH, Osborne JW. Validity and reliability of the neonatal skin condition score. J Obstet Gynecol Neonatal Nurs. 2004; 33(3):320-7.
17. García-Fernández FP, Pancorbo-Hidalgo P, Soldevilla Agreda JJ. Escalas de valoración del riesgo de desarrollar úlceras por presión en la infancia. Gerokomos. 2011; 22 (1):26-34.
18. Chattas G. Guía de práctica clínica para el cuidado de la piel del recién nacido, FUNDASAMIN. 2018:58-60.[Consulta: 06-03-21]. Disponible en: https://drive.google.com/file/d/1pTE5UOiyTKjnjpTFBTxTqp94bRL4iu-FA/view.
19. Hadfield G, De Freitas A, Bradbury S. Clinical evaluation of a silicone adhesive remover for prevention of MARSI at dressing change. Journal of Community Nursing. 2019; 33(3):36-41.
20. Schultz GS, Sibbald RG, Falanga V, Ayello EA, et al. Wound bed preparation: a systematic approach to wound management. Wound Repair Regen 2003; 11 (Suppl 1):S1-28.
21. Kimberly Leblanc K, Baranoski S, Christensen D, et al. The Art of Dressing Selection: A Consensus Statement on Skin Tears and Best Practice. Adv Skin Wound Care 2016; 29(1):E1-E2.
22. Martínez-Correa E, Osorio-Delgado MA, Henao-Tamayo LJ, Castro-Herazo CI. Clasificación Sistemática de Apósitos: Una Revisión bibliográfica. Rev Mex Ing Bioméd. (Internet). 2020; 41(1):5-28.













